El término diagnóstico prenatal comprende todas las modalidades de diagnóstico dirigidas a detectar durante la gestación una anomalía congénita que incluya trastornos estructurales o funcionales.
Aunque la mayoría de malformaciones (50-60%) son de causa desconocida. Se estima que un 25% puede deberse a factores genéticos. Las alteraciones genéticas que se identifican en el diagnóstico prenatal se pueden clasificar en 3 grandes grupos: cromosomopatías numéricas o estructurales, enfermedades monogénicas y enfermedades poligénicas/multifactoriales.
Para el diagnóstico de estas alteraciones genéticas se utilizan tanto técnicas citogenéticas como moleculares. Además, se han desarrollado técnicas que no necesitan realizar cultivos celulares para el diagnóstico rápido de las cromosomopatías más frecuentes. Entre ellas destaca la reacción en cadena de la polimerasa cuantitativa y fluorescente (QF-PCR) y la hibridación in situ fluorescente (FISH).
El Estudio de las alteraciones genéticas en el periodo prenatal se viene realizando con muestras obtenidas mediante una técnica invasiva (TI), bien biopsia corial, que se obtiene entre las semanas 11-14 de gestación, amniocentesis a partir de la semana 15 y cordocentesis a partir de la semana 20. Estas pruebas conllevan un riesgo de pérdida fetal que se estima alrededor del 0,1% en la amniocentesis, del 0,2% en la biopsia corial y del 3-5% en la cordocentesis.
Además de las técnicas invasivas mencionadas, hay que destacar aquellas no invasivas como son el cribado prenatal combinado del primer o segundo trimestre y la reciente incorporación del test prenatal no invasivo (TPNI), el cual se lleva a cabo con una muestra de sangre materna, permitiendo la detección del riesgo de las trisomías más frecuentes (21, 18 y 13) y de las cromosomopatías X e Y en el ADN fetal que circula en sangre materna.
Indicaciones para la realización del test prenatal no invasivo (TPNI)
El TPNI, por su mayor valor predictivo positivo respecto al cribado combinado del primer trimestre, se aplica de forma contingente como prueba de segundo nivel para los embarazos con riesgo de aneuploidías en el cribado combinado del primer o segundo trimestre o embarazos con riesgo de aneuploidías por antecedentes de nacido, aborto o interrupción voluntaria del embarazo con cromosomopatías.
Es importante señalar que el TPNI solo esta validado como método de cribado de estas alteraciones genéticas, pero no para ser empleado como confirmación diagnóstica, por lo que cualquier resultado positivo con TPNI debe ser confirmado mediante una prueba invasiva. En las pacientes con índices de riesgo muy elevados en el cribado combinado (superior a 1:50), se recomienda realizar directamente la prueba invasiva, ya que en esta población de gestantes es mayor el porcentaje de alteraciones genéticas que no se detectan por TPNI.
Indicaciones para la realización de pruebas invasivas
Las técnicas invasivas no están exentas de complicaciones y conllevan cierto riesgo de interferir en la evolución de la gestación, por lo que es esencial seleccionar las gestaciones que pueden beneficiarse de su realización. Entre ellas encontramos: a) Progenitor(es) portador(es) o afectado(s) de enfermedades hereditarias mendelianas o monogénicas; b) Progenitor(es) portador(es) de alteraciones cromosómicas; c) Riesgo ≥ 50 en el cribado combinado de primer o cribado bioquímico de segundo trimestre; d) TPNI con alto riesgo para trisomía 21, 18 y 13; e) TN ≥ P99 (o ≥ 3,5 mm) en la ecografía del primer trimestre; f) Hidropesía no inmune (HNI); g) Presencia de malformaciones fetales; h) Restricción del crecimiento intrauterino precoz (< semana 24) o severo (P < 3); i) Riesgo de infección fetal; j) Confirmación de un diagnóstico genético preimplantacional (DGP).
Técnicas de análisis para la detección prenatal de alteraciones genéticas
- Cariotipo
El cariotipo (estudio cromosómico de células en metafase) fetal se lleva a cabo mediante el análisis de células in vitro obtenidas con una prueba invasiva, pudiendo realizarse mediante análisis directo o con células procedentes de cultivo. Actualmente, la biopsia corial y la amniocentesis son las TI más utilizadas, sin embargo, hay que tener en cuenta una posible contaminación de la muestra con células de origen materno tanto por líquidos amnióticos hemáticos como en muestras de vellosidades coriales contaminadas con decidua materna.
Las muestras de líquido amniótico no contienen células fetales en división y tienen que cultivarse in vitro mediante un cultivo largo para poder obtenerlas en metafase, convirtiéndose, el tiempo de cultivo celular, en el factor limitante de la técnica. Tanto en el caso de vellosidad corial como de líquido amniótico el cultivo implica un tiempo mínimo de 8-10 días. Como alternativa se podría realizar un cultivo corto, de 24-48h, sin embargo, las metafases obtenidas serán de baja calidad.
- QF-PCR y FISH
Se trata de los dos métodos moleculares más empleados en muestras invasivas para el diagnóstico prenatal rápido de las enfermedades cromosómicas. Es importante destacar que estas técnicas normalmente se diseñan para detectar alteraciones genéticas solo en los cromosomas 13, 18, 21, X e Y, que son los más frecuentemente implicados en las aneuploidias, y que permiten ofrecer un resultado en 24-48h. Se pueden realizar tanto en líquido amniótico como en vellosidad corial.
La QF-PCR es una técnica citogenético-molecular que analiza regiones altamente polimórficas de los cromosomas (STR). Consiste en la realización de una PCR múltiple utilizando oligonucleótidos marcados con fluorocromos específicos de STR localizados en los cromosomas 21, 18, 13, X e Y.
La FISH consiste en la hibridación de secuencias de ADN cromosómicas específicas marcadas con fluorocromos en una preparación cromosómica.
Frente a la FISH, la QF-PCR presenta varias ventajas: a) La FISH requiere más volumen de muestra y mayor tiempo de análisis; b) La FISH no permite determinar la presencia de contaminación materna mientras que la QF detecta picos extras o ratios sesgados entre alelos. Por su parte, la FISH tiene la ventaja de permitir descartar/confirmar mosaicos analizando un elevado número de células, mientras que la QF no detecta mosaicos por debajo del 30%.
- Microarrays cromosómicos
La tecnología de microarrays cromosómicos (CMA) permite detectar cambios en el número de copias (deleciones y duplicaciones) a lo largo de todo el genoma con alta resolución y rapidez.
En cuanto al tipo de muestra, es posible realizar CMA tanto en biopsia de vellosidades coriales, líquido amniótico, sangre u otro tejido fetal. La muestra más habitual suele ser líquido amniótico, ya que se realiza a partir de la semana 15. En paralelo a la extracción de ADN se recomienda realizar un cultivo celular para realizar cariotipo u otras técnicas en caso necesario.
La realización de CMA en diagnóstico prenatal estaría indicada en los siguientes casos:
- Hallazgos ecográficos. TN superior al percentil 99, hallazgo ecográfico asociado a un síndrome concreto o hallazgo ecográfico inespecífico (malformación ecográfica o retraso de crecimiento intrauterino severo (< P3) y precoz (< 24 semanas)).
- Antecedentes personales o familiares. Presencia de deleción o duplicación familiar críptica o antecedentes familiares de reordenamiento cromosómico en equilibrio.
- Presencia en cariotipo fetal de un reordenamiento aparentemente equilibrado de novo o un cromosoma marcador.
Entre las limitaciones que presenta el CMA se encuentran: no detecta mutaciones puntuales, expansiones de tripletes, reordenamientos equilibrados ni mosaicismos de bajo grado o compensados.
Algoritmo diagnóstico
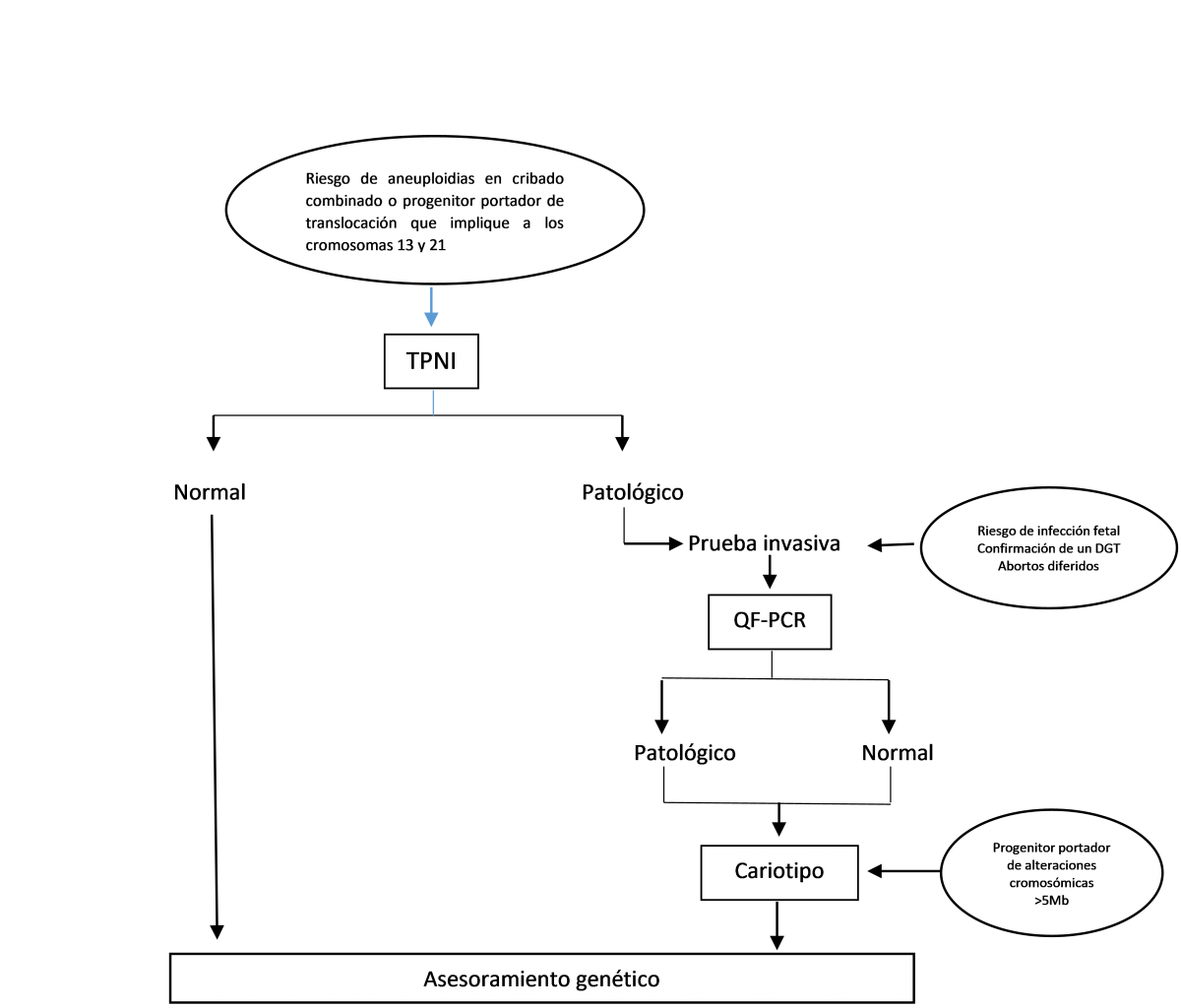
AUTOR • Dr. José Saura • Facultativo Especialista en Bioquímica Clínica en el laboratorio Analiza • Hospital Marina Salud Denia

 English
English Português
Português
¿Quieres recibir noticias como ésta en tu email?
Suscríbete a la newsletter